目前在新藥開發的臨床前試驗是以動物實驗及二維細胞培養為主,但動物實驗常因基因上的差異,在進入人體試驗階段才發現藥物功能低下或具細胞毒性而必須撤回。二維細胞培養則因缺乏體內的三維結構及微生理環境,因此其所獲得量化數據與實際體內藥物投遞機制有所出入。由於以上這兩種限制,開發中的藥物有高達90%以上的比例無法通過認證,造成醫藥成本及時間的耗損。因此,為能有效縮短藥物開發時間,以及降低成本,具有代表性的人體器官及疾病模型是目前極需的臨床前試驗開發平台,以簡化、加速、及精準地達到藥物開發、篩選、及確認毒性的工作。
本團隊多年來投入人類血管化腫瘤晶片的開發,此技術是將微流道系統類比成阻抗電路,組織培養腔室類比成附載阻抗,如圖1A,開發出可使用單一淨水壓控制一具雙腔室腫瘤晶片裝置的微生理環境,可在兩腔室中分別培養人類血管組織與腫瘤組織,藉由生理環境的控制,讓初期培養中的內皮細胞可在不受腫瘤組織影響下發展成正常的微血管網絡,待兩個組織各自發展完成後即可進行交互作用,自動進入腫瘤血管新生步驟,培養出具血管網絡之人類腫瘤體外模型,如圖1B。此腫瘤晶片提供可模擬體內透過血管投遞藥物的人體腫瘤微環境模型,成功突破以一般培養皿培養腫瘤細胞或腫瘤細胞球所欠缺的體內動態微生理環境的根本問題。為驗證此腫瘤裝置的功能性,本團隊使用化療藥物進行的此腫瘤晶片的藥物篩檢的功能測試,如圖1C,成功驗證以此裝置做為臨床前試驗的人體腫瘤模型的可行性。
最後,本研究亦提出,在晶片中培養腫瘤組織需在不同階段提供不同的微生理環境,在培養初期須將腫瘤對周圍正常組織的影響控制到最低,降低反血管因子對發展中之正常血管組織的影響,而在後期當血管組織已經完成生長,則再藉由微生理環境的操控,讓已發展完成的正常組織與腫瘤組織相互作用,才能發展出具有相當代表性之血管化人類腫瘤組織模型。(應力所許聿翔教授提供)
參考文獻:
1. Hsu YH, Yang WC, Chen YT, Lin CY, Yang CF, Liu WW, Shivani S, Li PC. Spatially controlled diffusion range of tumor-associated angiogenic factors to develop a tumor model using a microfluidic resistive circuit. Lab Chip. 2024 May 14;24(10):2644-2657.
DOI: 10.1039/d3lc00891f.
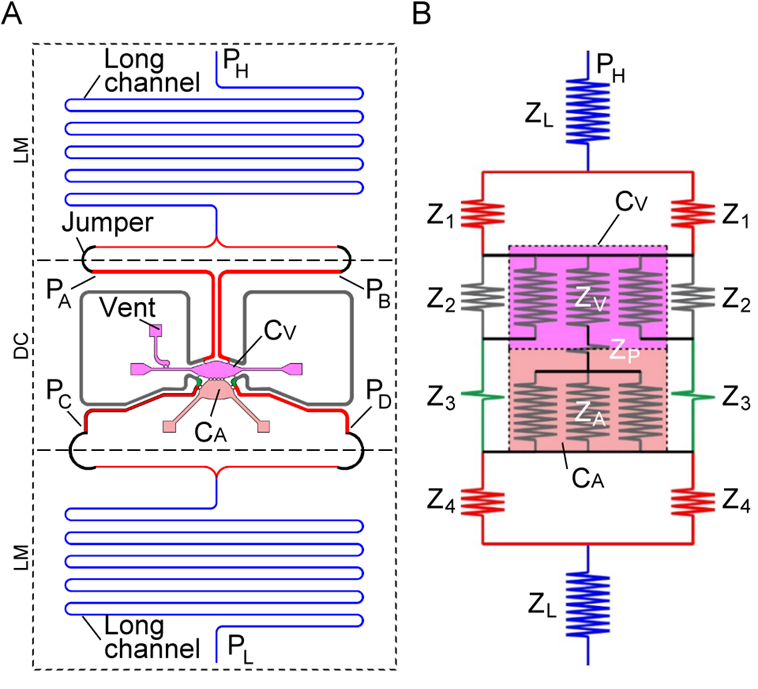
圖1、本團隊所開發之腫瘤晶片微流道系統(A)及其等校電路(B)[1]。
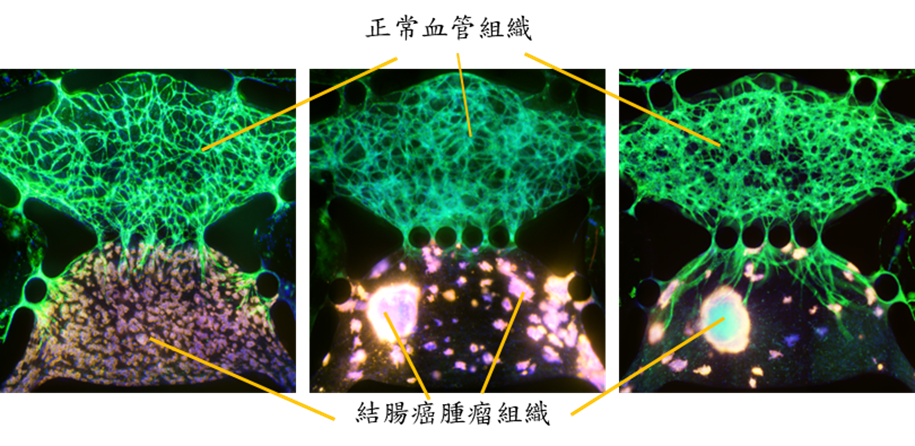
圖2、具有血管網絡之體外人類腫瘤組織模型[1]。
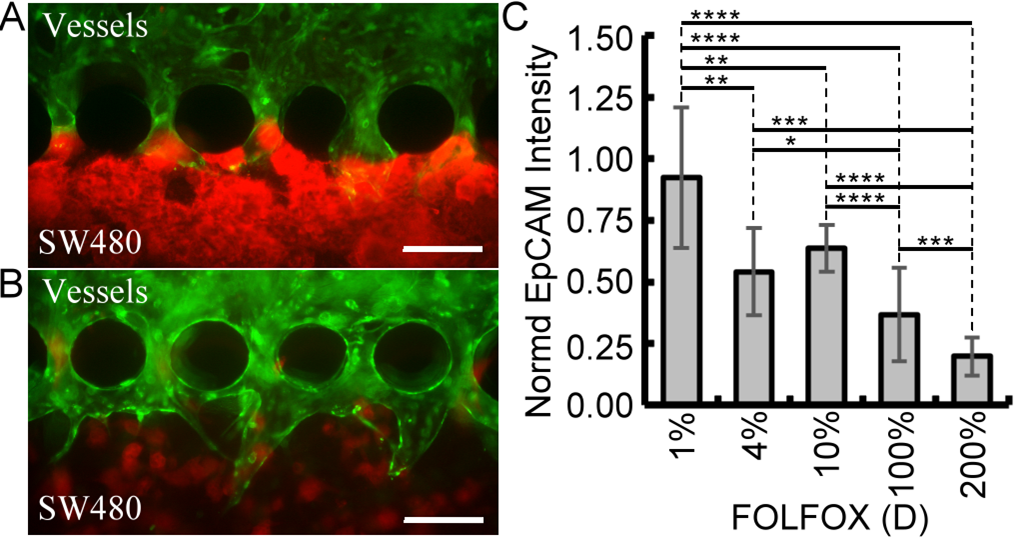
圖3、使用FOLFOX化療藥物對具血管化SW480結腸癌細胞的200%(A)及4%(B)
藥物濃度投藥結果,以及FOLFOX藥物的功能性篩藥結果(C)[1]。